本品为人血液制品,因原料来自人血,虽然对原料血浆进行了相关病原体的筛查,并在生产工艺中加入了去除和灭活病毒的措施,但理论上仍存在传播某些已知和未知病原体的潜在风险,临床使用时应权衡利弊。
>国内首家血液制品GMP认证企业
>国内首家采用双重病毒灭活工艺用于生产
>国内首家采用全自动采浆机和全自动洗瓶灭菌罐装生产线的生产企业
>血浆优质安全,多道ELISA(酶联免疫法)和核酸扩增技术检测
>不含防腐剂和抗生素,纯度高,稳定性好
>全面与世界接轨的标准化体系认证

请仔细阅读说明书并在医师指导下使用
本品为人血液制品,因原料来自人血,虽然对原料血浆进行了相关病原体的筛查,并在生产工艺中加入了去除和灭活病毒的措施,但理论上仍存在传播某些已知和未知病原体的潜在风险,临床使用时应权衡利弊。

[药品名称]
通用名称:人纤维蛋白粘合剂
商品名称:康普欣
英文名称:Human Fibrin Sealant Kit
汉语拼音:Ren Xianwei Danbai Nianheji
[成份]
本品主要成份由外用人纤维蛋白原(成份I) 、外用人纤维蛋白原稀释剂(成份II)、外用冻干人凝血酶(成份III)、外用冻干人凝血酶稀释剂(成份IV )组成。
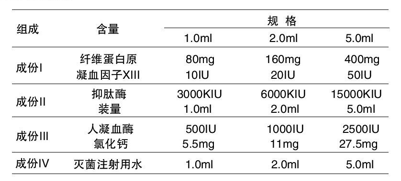
其中外用人纤维蛋白原内辅料为:蔗糖、甘氨酸、精氨酸、枸橼酸钠;外用冻干人凝血酶内的辅料为:氯化钠、蔗糖、甘氨酸、氯化钙葡萄糖酸钠、人血白蛋白。
[性状]
本品由外用人纤维蛋白原、外用冻干人凝血酶及相应稀释剂组成,其中外用人纤维蛋白原为白色或淡黄色疏松体,无融化迹象,溶解后为澄明或带轻微乳光的溶液。外用冻干人凝血酶为白色、灰白色或淡黄色疏松体,无融化迹象,溶解后为无色澄明或带轻微乳光的溶液,本品不含任何防腐剂。
[适应症]
用于烧伤及普通外科手术中局部止血的辅助处理。
[规格]
1.0ml/套
[用法用量]
根据“人纤维蛋白粘合剂配制及使用方法”图示,用台下注射器1抽吸外用人纤维蛋白原稀释剂(图1),注入外用人纤维蛋白原瓶内,得外用人纤维蛋白原溶液(图3);用台下注射器2抽吸外用冻干人凝血酶稀释剂(图2),注入外用冻干人凝血酶瓶内,得冻干人凝血酶溶液(图4)。用台上注射器1抽吸外用人纤维蛋白原溶液(图5),台上注射器2抽吸外用冻干,人凝血酶溶液(图6)。两注射器内的液体一定要等容量,并不要留有气泡。然后将它们分别卡入双联注射架上。再把Y型转换器安装到连接针座的锥头上,将平头针或喷嘴连接到Y型转换器上。安装完毕后,检查无松动渗漏,匀速、均衡的推动注射器联杆,点布或喷涂到需要处理的组织创面上,即可形成纤维蛋白粘合剂。
涂粘合剂之前,吸干伤口表面,提供一个干爽的表面,然后沿着缝线或创面处涂粘合剂,10秒内就会开始凝固。涂上胶体后,最少在60秒内不要吸干或压迫伤口。
使用的剂量与所要粘合或覆盖的表面、使用的涂药方法有关,用1.0ml规格的人纤维蛋白粘合剂可以粘合面积大约为10cm²的创面。
[注意]
1.请使用与本品配套的注射器和注射针分别溶解、抽吸相应的制品和溶液;
2.制备纤维蛋白原溶液的器具绝对不能与制备凝血酶溶液的混用,以免凝胶提前形成;
3.外用人纤维蛋白原溶解时,先将制品及其稀释剂的温度平衡至30~37°C,注入该稀释剂后静置1 - 2分钟,再轻轻转动,至冻干制剂完全溶解,以避免产生泡沫。
4.用Y型转换器牢固地将两个注射器和平头针或喷嘴连接一起;
5.使用过程中,若发现平头针针管或喷嘴被蛋白凝块阻塞,请更换一个新的平头针或喷嘴;
6.一旦开始输送胶体,就不能往回拔针管活塞,否则会使粘合剂回到“Y"型转换器中。这就会堵塞涂药器的尖端,需要再打开一个新的“Y"型转换器。
[不良反应]
在对牛蛋白质高度敏感或重复使用情况下可能会出现过敏反应,但十分罕见,如果出现症状,应立即停止用药,反应严重需要治疗的可以采取注射抗组织胺和类皮质激素药物。如发现过敏休克,则应立即注射肾上腺素(慢静脉注射),加高剂量类皮质激素(慢静脉注射),恢复血容量、氧。
[禁忌]
已知对牛蛋白质高度敏感者禁用。
[注意事项]
1.本品严禁静脉给药,仅供局部使用;
2.配置好的溶液在4小时内使用;
3.避免本品和消毒剂中的酒精、碘或其它重金属接触后,引起变性,所以涂两种成分之前应去掉伤口表面所有杂质。
[孕妇及哺乳期妇女用药]
孕妇及哺乳期患者用药应十分谨慎。
[儿童用药]
未专门进行该项针对性试验研究,且无系统可靠的参考文献。
[老年用药]
未专门进行该项针对性试验研究,且无系统可靠的参考文献。
[药物相互作用]
未专门进行该项针对性试验研究,且无系统可靠的参考文献。
[药物过量]
在国外同类型产品临床使用过程中,至今尚未发现任何药物过量导致的副反应,过量的药物大约在15天内被自身的纤溶酶快速水解和吸收。
[致栓危险]
在国外同类型产品临床使用过程中,至今尚未发现任何致栓的报导。如无意的静脉使用可能造成血栓并发症,因此严禁静脉使用。严重的动脉和静脉出血,这种大出血需要额外的措施。
[药理毒理]
本品主要由人血浆制备的纤维蛋白原/FXIII浓缩物和凝血酶浓缩物组成,在两种成份混合时,模拟凝血链级反应的最后一步,通过凝血酶对纤维蛋白原的激活作用,使纤维蛋白原逐渐聚合,最终形成纤维蛋白固化物,起到术前和术后止血和组织粘合作用。
[药代动力学]
未专门进行该项针对性试验研究,且无系统可靠的参考文献。
[贮存]
严格于2~8°C避光保存和运输,严禁冰冻。
[包装]
硼硅玻璃管制注射剂瓶、溴化丁基橡胶塞包装。1套/盒。 1套包含:外用人纤维蛋白原1瓶;外用人纤维蛋白原稀释剂1瓶外用冻干人凝血酶1瓶外用冻干人凝血酶稀释剂1瓶;配制药液所需的无菌注射器两支(台下附件)。医用材料包一个(台上附件),内含:双联注射架1支,推杆1支,5 ml注射器2支,复式注射座(即Y形转换器)2支,喷嘴2支,平头针2支,备用注射尖头针2支。
[有效期]
自外用人纤维蛋白原可凝性纤维蛋白原含量测定合格之日起24个月。
[执行标准]
WS4-(S-003)-2014Z
[批准文号]
国药准字S20020084
[生产企业]
企业名称:华兰生物工程股份有限公司
生产地址:中国河南省新乡市华兰大道甲1号
邮政编码:453003
电话号码:(0373) 3519992
传真号码:(0373) 3519991
网址:htp://ww.hwalanbio.com